Trong thế giới vi mô của các nguyên tử và phân tử, việc xác định khối lượng trở thành một thách thức lớn. Để đơn giản hóa quá trình này và tạo ra một hệ thống đo lường thống nhất, các nhà khoa học đã đưa ra khái niệm một đơn vị khối lượng nguyên tử (1 amu) theo định nghĩa có giá trị bằng một chuẩn mực nhất định. Việc hiểu rõ về đơn vị đo lường cơ bản này là chìa khóa để khám phá sâu hơn về cấu tạo vật chất và các phản ứng hóa học.
Nhu Cầu Về Một Đơn Vị Đo Khối Lượng Đặc Thù
Thế giới tự nhiên bao gồm vô số loại vật chất khác nhau, từ những vật thể khổng lồ đến những hạt siêu nhỏ mà mắt thường không thể nhìn thấy. Trong số đó, nguyên tử là đơn vị cấu tạo cơ bản của mọi vật chất, và việc hiểu được khối lượng của chúng là một bước cực kỳ quan trọng trong khoa học. Tuy nhiên, khối lượng của một nguyên tử lại vô cùng nhỏ bé, đến mức sử dụng các đơn vị khối lượng thông thường như gram hay kilogram sẽ gây ra sự bất tiện và phức tạp trong tính toán.
Khối Lượng Nguyên Tử và Thách Thức Đo Lường
Hãy tưởng tượng rằng khối lượng của một nguyên tử hydrogen chỉ khoảng 1,67 x 10^-24 gram, một con số cực kỳ nhỏ bé và khó hình dung. Khi làm việc với các phản ứng hóa học hoặc các phép tính liên quan đến hàng tỷ tỷ nguyên tử, việc sử dụng những con số có nhiều chữ số 0 như vậy sẽ dẫn đến sai sót và làm chậm quá trình nghiên cứu. Các nhà khoa học cần một cách biểu diễn khối lượng nguyên tử một cách thuận tiện hơn, giúp họ dễ dàng so sánh và tính toán tương đối giữa các nguyên tử khác nhau.
Sự Ra Đời của Đơn Vị Amu
Chính vì lý do đó, khái niệm về đơn vị khối lượng nguyên tử, hay viết tắt là amu (atomic mass unit), đã được giới thiệu. Đây là một đơn vị đo lường chuyên biệt, được thiết kế để diễn tả khối lượng của các nguyên tử và hạt hạ nguyên tử một cách hiệu quả hơn. Thay vì sử dụng những con số lũy thừa của 10, amu cho phép chúng ta làm việc với các giá trị nhỏ gọn và dễ quản lý hơn, mở ra cánh cửa cho những tiến bộ vượt bậc trong lĩnh vực hóa học và vật lý.
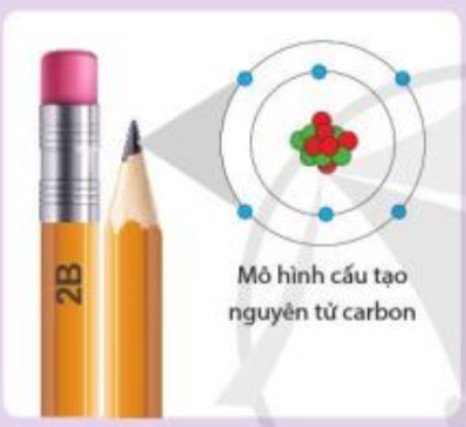
alt: Mô hình nguyên tử Hydrogen và Carbon theo Bo, minh họa cấu trúc nguyên tử và khái niệm đơn vị khối lượng nguyên tử (amu)
Định Nghĩa Chính Thức của Một Đơn Vị Khối Lượng Nguyên Tử (1 amu)
Để đảm bảo tính chính xác và nhất quán trong khoa học, việc định nghĩa một đơn vị khối lượng nguyên tử (1 amu) theo định nghĩa có giá trị bằng một tiêu chuẩn cụ thể là vô cùng quan trọng. Tiêu chuẩn này phải được chấp nhận rộng rãi và có thể tái tạo ở bất cứ đâu trên thế giới. Sau nhiều lần thay đổi và thảo luận, các nhà khoa học đã thống nhất sử dụng đồng vị carbon-12 làm chuẩn mực.
Tiêu Chuẩn Nguyên Tử Carbon-12
Theo định nghĩa hiện đại, một đơn vị khối lượng nguyên tử (1 amu) theo định nghĩa có giá trị bằng chính xác 1/12 khối lượng của một nguyên tử carbon-12 trung hòa điện. Nguyên tử carbon-12 được chọn làm chuẩn vì nó là một đồng vị phổ biến, ổn định và dễ dàng kiểm soát trong các thí nghiệm. Việc định nghĩa dựa trên một nguyên tử cụ thể giúp loại bỏ sự mơ hồ và đảm bảo rằng giá trị của amu luôn nhất quán. Nguyên tử carbon-12 chứa 6 proton, 6 neutron và 6 electron.
Giá Trị Cụ Thể của 1 Amu trong Hệ SI
Khi quy đổi sang hệ đơn vị quốc tế (SI), một đơn vị khối lượng nguyên tử (1 amu) theo định nghĩa có giá trị bằng xấp xỉ 1.66053906660 × 10^-27 kilogam (hoặc 1.66053906660 × 10^-24 gram). Giá trị này được xác định một cách chính xác thông qua các phép đo vật lý phức tạp, cho phép các nhà khoa học liên kết thế giới nguyên tử với các đơn vị đo lường vĩ mô mà chúng ta vẫn thường sử dụng trong cuộc sống hàng ngày. Việc nắm rõ con số này giúp chúng ta chuyển đổi giữa các đơn vị và thực hiện các tính toán chuyên sâu trong nhiều lĩnh vực khoa học khác nhau.
 Bảng thống kê thông tin các hạt trong nguyên tử
Bảng thống kê thông tin các hạt trong nguyên tử
Tầm Quan Trọng của Đơn Vị Khối Lượng Nguyên Tử trong Hóa Học
Đơn vị amu không chỉ là một khái niệm trừu tượng mà còn là một công cụ thiết yếu, giúp các nhà khoa học hiểu rõ hơn về cấu trúc và hành vi của vật chất ở cấp độ nguyên tử. Nó tạo ra một ngôn ngữ chung, cho phép các nhà khoa học trên toàn thế giới trao đổi thông tin và kết quả nghiên cứu một cách hiệu quả. Nhờ có amu, việc tính toán và dự đoán các tính chất hóa học trở nên đơn giản và chính xác hơn rất nhiều.
Tính Toán Khối Lượng Phân Tử và Phản Ứng
Trong hóa học, việc tính toán khối lượng phân tử của một chất là một bước cơ bản. Bằng cách cộng khối lượng nguyên tử (tính bằng amu) của tất cả các nguyên tử cấu thành một phân tử, chúng ta có thể dễ dàng xác định khối lượng tổng thể của phân tử đó. Ví dụ, một phân tử nước (H2O) có khối lượng khoảng 18 amu (16 amu của oxygen cộng với 2 lần 1 amu của hydrogen). Điều này giúp các nhà hóa học xác định tỷ lệ chất tham gia và sản phẩm trong các phản ứng hóa học, từ đó tối ưu hóa quy trình sản xuất hoặc tổng hợp các hợp chất mới.
Liên Hệ Với Các Hạt Cơ Bản (Proton, Neutron, Electron)
Đơn vị khối lượng nguyên tử cũng giúp chúng ta hiểu rõ hơn về khối lượng của các hạt hạ nguyên tử cấu tạo nên nguyên tử. Khối lượng của một proton và một neutron xấp xỉ 1 amu mỗi loại, trong khi khối lượng của một electron lại vô cùng nhỏ, chỉ khoảng 0.00055 amu. Điều này có nghĩa là gần như toàn bộ khối lượng của một nguyên tử tập trung ở hạt nhân, nơi chứa các proton và neutron. Sự chênh lệch khối lượng đáng kể này là lý do tại sao các electron thường bị bỏ qua khi tính khối lượng nguyên tử tổng thể của một nguyên tố.
 Sơ đồ cấu tạo nguyên tử Nhôm (Aluminum)
Sơ đồ cấu tạo nguyên tử Nhôm (Aluminum)
Các Thuật Ngữ Liên Quan và Cách Sử Dụng
Ngoài amu, đôi khi chúng ta còn bắt gặp các thuật ngữ khác như “Dalton” (Da) hoặc “khối lượng nguyên tử tương đối”. “Dalton” là một tên gọi khác cho đơn vị khối lượng nguyên tử và thường được sử dụng trong sinh hóa học để chỉ khối lượng của các đại phân tử như protein. Ví dụ, một protein có khối lượng 50.000 Da cũng có thể được nói là có khối lượng 50.000 amu. Đây là những thuật ngữ đồng nghĩa, phản ánh sự đa dạng trong cách diễn đạt nhưng cùng chỉ về một khái niệm cốt lõi: đơn vị khối lượng nguyên tử.
Khối lượng nguyên tử tương đối, mặt khác, là một con số không có đơn vị, được tính bằng cách lấy khối lượng nguyên tử của một nguyên tố (tính bằng amu) chia cho 1 amu. Ví dụ, nếu một nguyên tử có khối lượng là 12 amu, thì khối lượng nguyên tử tương đối của nó là 12. Điều này giúp chúng ta dễ dàng so sánh khối lượng của các nguyên tố khác nhau mà không cần bận tâm đến đơn vị đo. Việc hiểu rõ các thuật ngữ này giúp chúng ta giao tiếp và nghiên cứu khoa học một cách chính xác hơn.
FAQs về Đơn Vị Khối Lượng Nguyên Tử (amu)
1. Amu là viết tắt của từ gì?
Amu là viết tắt của “atomic mass unit”, có nghĩa là đơn vị khối lượng nguyên tử.
2. Tại sao lại cần có đơn vị amu thay vì chỉ dùng gram hoặc kilogam?
Đơn vị khối lượng nguyên tử (amu) được sử dụng để đo khối lượng của các nguyên tử và hạt hạ nguyên tử vì khối lượng của chúng quá nhỏ. Việc sử dụng gram hoặc kilogam sẽ dẫn đến những con số với rất nhiều chữ số 0, gây khó khăn và sai sót trong tính toán. Amu giúp đơn giản hóa các giá trị này.
3. Nguyên tử nào được dùng làm chuẩn để định nghĩa 1 amu?
Một đơn vị khối lượng nguyên tử (1 amu) theo định nghĩa có giá trị bằng chính xác 1/12 khối lượng của một nguyên tử carbon-12 trung hòa điện. Nguyên tử carbon-12 được chọn vì sự ổn định và phổ biến của nó.
4. Khối lượng của proton và neutron có bằng 1 amu không?
Khối lượng của một proton và một neutron xấp xỉ bằng 1 amu mỗi loại. Tuy nhiên, giá trị chính xác có một chút khác biệt nhỏ.
5. Electron có đóng góp đáng kể vào khối lượng nguyên tử khi tính bằng amu không?
Không, khối lượng của electron rất nhỏ (khoảng 0.00055 amu) và thường được bỏ qua khi tính khối lượng nguyên tử tổng thể của một nguyên tố.
Việc hiểu rõ về một đơn vị khối lượng nguyên tử (1 amu) theo định nghĩa có giá trị bằng một phần mười hai khối lượng của nguyên tử Carbon-12 là nền tảng quan trọng trong hóa học và vật lý. Hy vọng những thông tin này đã giúp bạn có cái nhìn toàn diện hơn về đơn vị đo lường cơ bản này. Tại Đồ Gỗ Vinh Vượng, chúng tôi luôn mong muốn mang đến những kiến thức hữu ích và đa dạng, dù là về khoa học hay những giá trị truyền thống, để làm phong phú thêm đời sống tinh thần của quý vị độc giả.

